Witamina D
Witamina D (ATC: A 11 CC 05) – grupa rozpuszczalnych w tłuszczach steroidowych organicznych związków chemicznych, które wywierają wielostronne działanie fizjologiczne, przede wszystkim w gospodarce wapniowo-fosforanowej oraz utrzymywaniu prawidłowej struktury i funkcji kośćca.
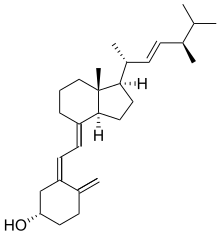

Podstawowe znaczenie mają dwie formy witaminy D, różniące się budową łańcucha bocznego:
- ergokalcyferol (witamina D2), naturalnie występujący w organizmach roślinnych/drożdżach
- cholekalcyferol (witamina D3), naturalnie występujący w organizmach zwierzęcych
Witaminy D w organizmie człowieka tradycyjnie zalicza się do witamin, jednak spełniają one funkcję prohormonów, ponieważ w wyniku przekształceń metabolicznych powstaje aktywna biologicznie postać – 1α,25-dihydroksycholekalcyferol.
W farmakoterapii witamina D znajduje zastosowanie przede wszystkim w profilaktyce i leczeniu krzywicy, osteomalacji i osteoporozy.
Biosynteza i metabolizm witaminy D u człowieka
edytujZarówno witamina D2, jak i D3 nie mają aktywności biologicznej. Uzyskuje je poprzez enzymatyczną hydroksylację przy tych samych atomach węgla ich cząsteczek. U ludzi biologicznie czynną formą witaminy D jest 1α,25-dihydroksywitamina D (1,25(OH)2D).
Prowitaminą D2 jest ergosterol, a D3 – pochodna cholesterolu 7-dehydrocholesterol. W skórze, przede wszystkim w naskórku (głównie w keratynocytach warstwy rozrodczej), pod wpływem światła słonecznego 7-dehydrocholesterol ulega nieenzymatycznej fotoizomeryzacji do prewitaminy D, która pod działaniem energii cieplnej ciała przekształcona zostaje w ciągu kilku godzin w witaminę D3[1].
Przekształcenie prowitaminy D w prewitaminę D zachodzi pod wpływem promieniowania UV o długości 290–315 nm (zakres UV-B), a eksperymentalnie ustalono, że najbardziej efektywną długością fali świetlnej jest 295–300 nm (z maksimum przy 297 nm).
Nie ma niebezpieczeństwa powstawania toksycznych ilości witaminy D3 w wyniku nadmiernej ekspozycji na światło słoneczne, ponieważ w takiej sytuacji nadmiar prewitaminy i witaminy jest rozkładany.
Ocenia się, że ok. 80–100% potrzebnej dla organizmu ilości witaminy D3 pochodzi z biosyntezy w skórze, a tylko w niewielkim stopniu wspomagane jest to przez źródła pokarmowe. Jednak na produkcję w skórze ma wpływ wiele czynników, m.in.: pora roku i dnia, zachmurzenie i zanieczyszczenia powietrza, szerokość geograficzna, stosowanie kremów z filtrem, powierzchnia ciała wystawiona na słońce, pigmentacja oraz starzenie się skóry. Skórna produkcja witaminy D często nie jest wystarczająca dla zaspokojenia dobowego zapotrzebowania przez większość dni w roku, szczególnie w krajach wysoko uprzemysłowionych.
Chole- i ergokalcyferol w połączeniu z białkiem wiążącym witaminę D są transportowane do wątroby, odpowiednio: z jelita cienkiego, gdzie są wchłaniane i ze skóry, gdzie cholekalcyferol jest produkowany. W wątrobie zachodzi pierwszy etap biosyntezy aktywnej postaci witaminy D. Po enzymatycznej hydroksylacji przy węglu C-25 powstaje witamina 25-(OH)D. Reakcję tę katalizuje prawdopodobnie zespół hydroksylaz wchodzących w skład cytochromu P450 (CYP27A1, CYP3A4 oraz CYP2R1)[2]. 25-(OH)D przekazywana jest, także w połączeniu z białkiem wiążącym witaminę D, z wątroby do nerek (a także do niektórych innych tkanek, np. skóry oraz komórek odpornościowych) gdzie przez działanie enzymu 1α-hydroksylazy (CYP27B1) dochodzi do powstawania aktywnej formy witaminy D – 1α,25-(OH)2D. Obie aktywne formy (1α,25-(OH)2D2 i 1α,25-(OH)2D3) charakteryzują się identycznymi własnościami, jednak ze względu na rozpowszechnienie częściej stosowana jest 1α,25-dihydroksycholekalcyferol (1,25-(OH)2D3), czyli kalcytriol.
Istnieje około 10 prowitamin, z których powstają związki wykazujące aktywność witaminy D. Przemysłowa produkcja witaminy D ogranicza się głównie do tych dwóch.
Ważnym metabolitem witaminy D jest 24R,25-dihydroksywitamina D, która powstaje w alternatywnym szlaku hydroksylacji 25(OH)-witaminy D.
Aktywność biologiczna
edytujGłówne działanie witaminy D polega na jej wpływie na regulację homeostazy wapnia i fosforanów. Dwa główne narządy efektorowe związane z tą funkcją, na które działają aktywne metabolity witaminy D to przede wszystkim jelita i kości, a w mniejszym stopniu nerki. W jelitach dochodzi do zwiększenia wchłaniania wapnia, z kości uwalnia wapń i fosforany (przy hipokalcemii) w nerkach współdziała z parathormonem w reabsorpcji wapnia.
Aktywne metabolity witaminy D charakteryzują się szerokimi i różnorodnymi działaniami biologicznymi. Aktywność witaminy D wywierana jest poprzez działania genomowe i niegenomowe. Witamina D w wielu tkankach i komórkach łączy się z jądrowym receptorem witaminy D (VDR), a następnie tworzy heterodimer z receptorem kwasu 9-cis retinowego (RXR) o własnościach czynnika transkrypcyjnego, przez co zapoczątkowuje działania genomowe. Witamina D kontroluje ponad 200 genów[3].
Działania niegenomowe mediowane są przez zlokalizowany w błonie komórkowy receptor, który jest odmienny od receptora jądrowego i uruchamia wewnątrzkomórkowe szlaki metaboliczne modulujące działania wynikające z ekspresji genowej.
Działania witaminy D
edytujUkład kostny
edytujWitamina D wywiera znaczący wpływ na metabolizm kości – zwiększa w osteoblaście ekspresję RANKL, a ten z kolei aktywuje RANK w prekursorze osteoklasta, co prowadzi do powstania dojrzałego osteoklasta, który przez działanie resorpcyjne powoduje uwalnianie wapnia z kośćca. W okresie rozwojowym ma istotne znaczenie w kształtowaniu się kości i zębów. Niedobór witaminy D (hipowitaminoza, awitaminoza) u dzieci prowadzi do krzywicy, zaburzenia mineralizacji kości i zmniejszenia masy kostnej, a u dorosłych wywołuje bóle kostne[4][5], osteomalację i osteoporozę.
Witamina D może pomagać w zwalczaniu próchnicy przez układ odpornościowy, gdyż aktywuje białka obronne (np. katelicydyny)[6][7].
Układ nerwowy i mięśniowy
edytujNiski poziom witaminy D u pacjentów stosujących statyny korelował z występowaniem mialgii[8].
Istnieje związek między stężeniem witaminy D w osoczu a zaburzeniami snu[9][10]. Poziom witaminy D w osoczu ciężarnej kobiety może być powiązany z ryzykiem wystąpienia zaburzeń autystycznych u jej przyszłego dziecka[11].
Układ immunologiczny
edytujMa działanie immunomodulujące i pośrednio przeciwbakteryjne. Witamina D aktywuje geny kodujące peptydy przeciwbakteryjne (o cechach naturalnych antybiotyków), katelicydynę i β-defensynę 2[12]. Katelicydyna wykazuje aktywność biologiczną przeciw wielu bakteriom, w tym bakteriom gruźlicy, co może tłumaczyć skuteczność „słonecznej kuracji” zalecanej w XIX wieku w leczeniu tej choroby. Katelicydyna jest produkowana przez komórki odpornościowe przy zetknięciu ze ścianami komórkowymi bakterii, w obecności formy 25D witaminy D[13].
W stwardnieniu rozsianym – W 2017 roku FDA wydało oświadczenie w którym stwierdza brak dostatecznych dowodów na stwierdzenie powiązania między spożyciem witaminy D a ryzykiem zapadnięcia na stwardnienie rozsiane u osób zdrowych[14]. Witamina D może być jednym z czynników powodujących sezonowe nawroty objawów stwardnienia rozsianego[15].
Ma działanie antyproliferacyjne i zapobiega powstawaniu komórek nowotworowych, wpływa na apoptozę i angiogenezę[3].
Według badań przeprowadzonych na 17 tys. osób wyższy poziom witaminy D w surowicy nie wpływa na całkowitą liczbę zgonów z powodu raka, choć osoby z wyższym poziomem mają niższe ryzyko zachorowania na raka jelita grubego[16].
Analiza 18 wyników badań, w których łącznie uczestniczyło 57 tys. ludzi, wykazała, że wśród przyjmujących witaminę D, w średniej dawce 528 j.m., śmiertelność spadła o 7%[17].
Niektóre badania wskazują, że witamina D może zmniejszać ryzyko zachorowania na grypę. Sezonowa zmienność zawartości witaminy D w organizmie (spowodowana zmiennością nasłonecznienia w różnych porach roku) wiąże się także, według tych badań, z sezonowością zakażeń na tę chorobę[18][19].
Układ krążenia
edytujBadania naukowe nie wykazują jednoznacznego wpływu witaminy D na nadciśnienie tętnicze[20][21].
Suplementacja witaminą D3 i wapniem moduluje stan zapalny w przewlekłej niewydolności serca[22].
Działania metaboliczne w wielu tkankach
edytujWitamina D stymuluje zdolność do regeneracji wątroby. Poprzez wpływ na jej funkcje antyproliferacyjne, nasilające różnicowanie i apoptozę oraz antyangiogeniczne, może działać przeciwnowotworowo[potrzebny przypis].
Właściwości chemiczne
edytujPierwotnie stosowano nazwę witamina A (od antirachitic – przeciwkrzywicza), ponieważ zauważono, że chroni przed krzywicą i osteoporozą oraz pomaga w leczeniu tych chorób[potrzebny przypis].
Witamina D posiada wspólny dla steroidów rdzeń cyklopentanoperhydrofenatrenowy, z tą różnicą, że pierścień B uległ rozszczepieniu. Nie rozpuszcza się w wodzie, ale jest rozpuszczalna w tłuszczach. Jest dość odporna na działanie podwyższonej temperatury. Nie ulega rozpadowi w czasie długotrwałego przechowywania, o ile zostaną zapewnione odpowiednie warunki (m.in. brak ekspozycji na promieniowanie UV). Ponadto jest stosunkowo trwała w środowisku zasadowym i zarazem wrażliwa na działanie kwasów. Ergokalcyferol ogrzewany powyżej temperatury 160–190 °C przechodzi w biologicznie nieaktywne izomery[potrzebny przypis].
Prowitaminą D2 jest ergosterol, a prowitaminą D3 jest 7-dehydrocholesterol.
Źródła witaminy D
edytujŹródła pokarmowe
edytujPod wpływem światła słonecznego w drożdżach i roślinach powstaje ergokalcyferol.
Najwięcej cholekalcyferolu zawiera mięso niektórych ryb (łosoś, dorsz, tuńczyk, śledź, makrela, sardynki, węgorz i inne) oraz tran. Ważnymi źródłami cholekalcyferolu są: wątroba, ser, żółtko jaj i niektóre grzyby.
W celu zapobieżenia ewentualnym niedoborom witaminy D niektóre produkty spożywcze są w nią wzbogacane. W USA: mleko i jogurt, płatki śniadaniowe, sok pomarańczowy oraz margaryna. W krajach europejskich są to: margaryna i płatki śniadaniowe. W Polsce obligatoryjnie margaryny wzbogaca się w witaminy A i D.
| Nazwa produktu | Zawartość witaminy D (1 j.m. = 0,025 µg) |
|---|---|
| węgorz świeży | 1200 j.m./100 g |
| śledź marynowany | 480 j.m./100 g |
| śledź w oleju | 808 j.m./100 g |
| dorsz świeży | 40 j.m./100 g |
| łosoś (gotowany/pieczony) | 540 j.m./100 g |
| makrela (gotowana/pieczona) | 152 j.m./100 g |
| ryby z puszki (tuńczyk, sardynki) | 200 j.m./100 g |
| żółtko jajka | 54 j.m./żółtko |
| ser żółty | 7,6–28 j.m./100 g |
| mleko ludzkie | 1,5–8 j.m./100 ml |
| mleko krowie | 0,4–1,2 j.m./100 ml |
Biofotosynteza w skórze
edytujDobowe zapotrzebowanie
edytujUstalenie norm dziennego zapotrzebowania na witaminę D jest utrudnione, ponieważ jej ważnym źródłem (niekiedy zaspokajającym w 100% zapotrzebowanie) jest cholekalcyferol powstający w skórze, ale ilość powstałej w ten sposób witaminy D w znacznym stopniu zależy od pogody oraz od tego, jaką część skóry i przez ile czasu wystawia się na oddziaływanie promieni słonecznych. Różne instytucje zalecają różne dzienne normy doustnego spożywania witaminy D.
Polski Instytut Żywności i Żywienia zaleca następujące normy[24]:
- niemowlęta: norma zalecana 20 µg, poziom bezpieczny 10 µg
- dzieci (1-9 r.ż): 15 µg, poziom bezpieczny 10 µg
- młodzież i osoby po 60. rż.: 10 µg, poziom bezpieczny 5 µg
W Unii Europejskiej oficjalnie zaleca się spożywać dziennie 5 µg witaminy D[25].
FDA zaleca spożywanie 10 µg (400 j.m.) witaminy D na dobę u dzieci powyżej 4. r.ż. i dorosłych (przy diecie zawierającej 2000 kcal)[26]. Inna amerykańska instytucja naukowa (Institute of Medicine, Food and Nutrition Board) zaleca spożywanie na dobę 5 µg w wieku do 51. roku życia, 10 µg w wieku 51-70 i 15 µg powyżej 71. roku życia[27].
Dla osób powyżej 60 lat Międzynarodowa Fundacja Osteoporetyczna (ang. International Osteoporosis Foundation) zaleca poziom 25OHD w surowicy wynoszący 75 nmol/L (30 ng/ml) osiągnięty przez spożywanie 20–25 μg/dzień (800–1000 j.m./dzień). Do czasu ogłoszenia tych zaleceń w 2010 efektywność wyższych dawek w zapobieganiu upadkom i złamaniom nie została oceniona w badaniach klinicznych. U osób otyłych, z osteoporozą, o ograniczonej ekspozycji na słońce (obłożnie chorych, kalek), z zaburzeniami wchłaniania oraz u nie-Europejczyków może być koniecznym zwiększenie spożycia do 50 μg/dzień (2 000 j.m./dzień). U tych zagrożonych osób Fundacja zaleca pomiar 25OHD w surowicy i powtórzenie pomiaru po 3 miesiącach suplementacji w celu sprawdzenia, czy stężenie witaminy D osiągnęło pożądany poziom. 2,5 μg (100 j.m.) dodanej witaminy D zwiększy poziom 25OHD w surowicy o około 2,5 nmol/l (1,0 ng/ml)[28].
Poziom witaminy D
edytujPrzy odpowiednim nasłonecznieniu ilość witaminy D, która jest wytwarzana w skórze, jest na tyle wystarczająca, że nie trzeba czerpać jej dodatkowo ze źródeł pokarmowych (nie jest więc do końca witaminą). Ilość wytwarzanej witaminy D u ludzi podlega wahaniom sezonowym i zazwyczaj spada, im dalej na północ lub południe od strefy okołorównikowej teren jest położony. W strefie klimatu umiarkowanego ilość światła słonecznego dostarczana przez około połowę roku jest za mała, aby skóra człowieka mogła sama wytworzyć dostateczną ilość tej witaminy.
Witamina D krąży w organizmie głównie w postaci 25(OH)D3. Najbardziej aktywną biologicznie formą jest 1,25(OH)2D3, której poziom jest regulowany hormonalnie[29]. Z tego względu bardziej wiarygodne jest oznaczanie poziomu 25(OH)D3. W umiarkowanym niedoborze witaminy D, a także w trakcie leczenia stężenia 1,25(OH)2D3 mogą być fałszywie wysokie i wprowadzać w błąd, zaś w przypadku przedawkowania pozostawać w normie.
Według amerykańskich Narodowych Instytutów Zdrowia prawidłowy poziom witaminy D wynosi ≥20 ng/ml, wartości poniżej 12 ng/ml prowadzą do krzywicy i osteomalacji. Wartości utrzymujące się stale powyżej 50 ng/ml są uważane za potencjalnie toksyczne, jednak wielkość ta opiera się na małej liczbie danych[30].
Na wniosek rządów USA i Kanady Institute of Medicine (IOM), po przeglądzie literatury, w 2010 zarekomendował ten sam poziom co najmniej 20 ng/ml. Jest on osiągalny przy jej dziennym spożyciu 600 j.m. (15 μg) i 800 j.m. (20 μg) u osób starszych. IOM nie znalazł dowodów na rolę witaminy D w chorobach innych niż choroby kości[31]. Rekomendacje te spotkały się z krytyką, m.in. z tego powodu, że w jednym z badań, na których opierał się IOM, wśród ludzi z poziomem co najmniej 20 ng/ml, 8,5% ludzi miało słabo zmineralizowane kości. Amerykańskie Towarzystwo Endokrynologiczne określiło poziom poniżej 30 ng/ml jako niewystarczający, a poziom 40–60 ng/ml, wymagający dziennego spożycia 37,5–50 μg witaminy D, jako idealny dla stanu zdrowia układów niezwiązanych z układem kostnym[32].
Oznaczanie poziomu witaminy D
edytujNajczęściej, ze względów praktycznych dla celów diagnostyki laboratoryjnej oznacza się stężenie 25-OH-witaminy D w surowicy krwi. Jest to łączne stężenie 25-OH-D2 i 25-OH-D3. Uważa się, że to badanie najlepiej ocenia metaboliczny stan zasobów witaminy D. W diagnostyce laboratoryjnej do oznaczania stężenia witaminy D i jej metabolitów wykorzystuje się następujące metody:
- radioimmunologiczną
- radioimmunokompetencyjną
- chromatografii gazowej wysokociśnieniowej
Komercyjne testy wykorzystywane przez laboratoria mogą znacznie różnić się stopniem powinowactwa do badanych metabolitów, co niekiedy prowadzi do zaniżenia wyniku stężenia witaminy D we krwi[33].
Skutki niedoboru
edytujPrzyczynami niedoboru są: małe spożycie w połączeniu z małą ekspozycją na słońce (UVB) i różne zaburzenia, w tym rzadko dziedziczne, takie jak zaburzenia wchłaniania, choroby zakłócające przemianę witaminy D w wątrobie i nerkach, w jej aktywne biologicznie metabolity.
Awitaminoza grozi krzywicą u dzieci i młodzieży, rozmiękaniem kości (osteomalacja) i osteoporozą u dorosłych, złamaniami, skrzywieniami i zwyrodnieniami układu kostnego, zniekształceniami sylwetki, złym funkcjonowaniem układu nerwowego i mięśniowego, zapaleniem spojówek, stanami zapalnymi skóry, osłabieniem organizmu i zmniejszeniem odporności, pogorszeniem słuchu, osłabieniem i wypadaniem zębów oraz zwiększeniem się ryzyka chorób autoimmunologicznych, zwłaszcza cukrzycy typu I, choroby Leśniowskiego-Crohna, raka pęcherza moczowego, piersi, jelita grubego, okrężnicy i jajnika. Osoby z chorobą Parkinsona[34] i stwardnieniem rozsianym[34] mają niższe stężenie witaminy D w surowicy. Ponadto niskie stężenie witaminy D może wiązać się z występowaniem insulinooporności[35].
Skóra o ciemnej karnacji produkuje witaminę D około sześciu razy wolniej, na skutek pochłaniania promieniowania UV przez melaninę. Powoduje to, że osoby rasy czarnej mają przeważnie o połowę mniejsze stężenie witaminy D we krwi niż biali.
Dzienna dawka witaminy D u osoby o jasnej karnacji powstaje w trakcie 5-15 minutowej ekspozycji między godziną 10 a 15. Dorosła kobieta (o jasnej karnacji) podczas opalania w bikini, wytwarza około 10 tys. j.m. w czasie 15-20 min.
Obecnie trwają badania weryfikujące zalecane dzienne spożycie witaminy D.
Skutki nadmiaru
edytujNie jest możliwe wywołanie hiperwitaminozy przy zwykłej diecie lub intensywnej ekspozycji na promieniowanie ultrafioletowe. Nadmierna ilość promieni UV rozkłada witaminę D do suprasterolu, zapobiegając nadprodukcji. W niektórych chorobach np. sarkoidozie, gruźlicy czy idiopatycznej hyperkalcemii o wiele mniejsze dawki niewiele przekraczające dawki terapeutyczne (np. powyżej 1000 j.m. na dobę) mogą już spowodować objawy zatrucia. Poziom witaminy D przekraczający 200 ng/ml (500 nmoli/L) uważa się za potencjalnie toksyczny prowadzący do hiperkalcemii i hiperfosfatemii[36].
Górne dopuszczalne dobowe dawki witaminy D, które nie stanowią zagrożenia dla zdrowej populacji, są powszechnie przyjęte i akceptowane przez wszystkie towarzystwa naukowe o oddziaływaniu globalnym i lokalnym (np. The Endocrine Society, czy European Food Safety Authority). W okresie noworodkowym i niemowlęcym wynosi 1000 j., w okresie od 1. do 10. roku życia 2000 j., od 11. do 18. roku życia oraz u dorosłych 4000 j.[37]
Tolerowalny wyższy poziom przyjmowania witaminy D został określony na 4000 j.m. (100μg)[38].
Występujące objawy są związane z hiperkalcemią – nudności i wymioty, brak apetytu, zaparcia, osłabienie i łatwe męczenie się, nadmierne pragnienie, wzmożone oddawanie moczu, świąd skóry, bóle głowy. Przy towarzyszącej hiperkalciurii może dochodzić do tworzenia złogów nerkowych (kamica nerkowa), a także zwapnień (nefrokalcynoza), następnie do niewydolności nerek. Złogi wapniowe mogą pojawiać się w tkankach: np. tętnicach, sercu, płucach. U dzieci można zaobserwować opóźnienia w rozwoju psychomotorycznym.
Nadwrażliwość
edytujW przypadku występowania nadwrażliwości na witaminę D3, możliwe jest wystąpienie wyżej wymienionych skutków nadmiaru, mimo nieprzekroczenia potencjalnie toksycznego poziomu cholekalcyferolu. Do przyczyn nadwrażliwości występują idiopatyczna hiperkalcemia niemowląt (dziedziczona autosomalnie recesywnie), zespół Williamsa-Beurena, choroby ziarniniakowe i niektóre chłoniaki. Udowodniono także związek nadwrażliwości na witaminę D z licznymi mutacjami genetycznymi, np. w białkach kodujących kotransporter sodowo-fosforanowy[37].
Historia
edytujDo odkrycia doprowadziły badania nad krzywicą, dziecięcą chorobą kośćca, która była szeroko rozpowszechniona w miastach w czasach rewolucji przemysłowej. Na początku XIX wieku badacze wykryli, że lecznicze działanie u dzieci chorych na krzywicę ma promieniowanie ultrafioletowe i olej z wątroby dorsza.
Kąpiele słoneczne jako metodę leczenia krzywicy opisał, w 1822 roku, Jędrzej Śniadecki[39][40].
Przez stulecia medycyna ludowa stosowała tran jako remedium w leczeniu krzywicy. Na przełomie XIX i XX wieku badania naukowe skupiły się na wykryciu czynnika przeciwkrzywiczego w tranie. Odkrycia dokonał w 1922 r. McCollum, napowietrzając i ogrzewając go, rozłożył znajdującą się w nim substancję przeciwdziałającą kseroftamii (witamina A), pozostawiając nietknięte działanie przeciwkrzywicze tranu. Przez co udowodnił, że są to odmienne substancje chemiczne. Czynnik przeciwkrzywiczy został nazwany witaminą D[41].
Poprzez naświetlanie ergosterolu, sterolu uzyskanego z drożdży, otrzymano produkt, który nazwano witaminą D1, lecz później ustalono, że jest to w rzeczywistości mieszanina ergokalcyferolu i lumisterolu. W 1931 roku poprzez separację uzyskano z „witaminy D1” ergokalcyferol, czyli witaminę D2. Sądzono wówczas, że jest ona tożsama z witaminą wytwarzaną w skórze, jednak dalsze badania wykazały, że są to różne związki chemiczne. Dalsze badania wykazały istnienie prekursora witaminy D w skórze – 7-dehydrocholesterolu oraz doprowadziły w 1936 roku do odkrycia witaminy D3. Dalsze badania w 2. połowie XX wieku doprowadziły do szczegółowego poznania funkcji i metabolizmu witaminy D.
W roku 1968 wyizolowano pierwszy aktywny metabolit witaminy D, 25-hydroksywitaminę D3 (25OHD3)[42].
Preparaty
edytujW Polsce w profilaktyce i leczeniu stosuje się głównie cholekalcyferol, a np. w USA ergokalcyferol. Preparaty zawierające witaminę D (lub jej metabolity) są obecne na polskim rynku, głównie:
- w postaci cholekalcyferolu
- jako preparaty złożone cholekalcyferolu ze związkami wapnia lub ze związkami wapnia i innych składników
- preparaty złożone cholekalcyferolu z retinolem
- preparaty złożone cholekalcyferolu z phytomenadionem (witamina K)
- w postaci kalcytriolu
- w postaci alfakalcydolu
- w postaci kalcyfediolu
Dawkowanie
edytujDawki witaminy D stosowane są ustalane indywidualnie i zależą od konkretnej sytuacji klinicznej. Ze względu na ścisły związek poziomu witaminy D z poziomem wapnia, przed i w trakcie leczenia należy go monitorować.
Profilaktyka
edytujDoustne:
- dzieci po 4. tygodnia życia niemowlęta donoszone, prawidłowo pielęgnowane, przebywające często na świeżym powietrzu oraz dzieci do 2-3. roku życia – 500 j.m./dobę
- po 4. tygodnia życia u wcześniaków, bliźniąt i niemowląt żyjących w złych warunkach socjalnych 1000 j.m./dobę
- dorośli: 1000–4000 IU/d. lub 20 000–25 000 IU podawanych raz w tygodniu lub raz w miesiącu[43].
Leczenie
edytujLeczenie doustne:
- dorośli z niedoborem (<20 ng/ml 25(OH)D3): 40 000 IU/tydzień przez 7 tyg. lub 50 000 IU/tydzień przez 6 tyg.[43]
- od 4. tygodnia życia do 18. roku życia 3 000-10 000 j.m./dobę przez 4-6 tygodni pod ścisłą kontrolą lekarską (można powtórzyć po tygodniowej przerwie)
- w krzywicy i osteomalacji 1000-5000 j.m./dobę
- w osteoporozie 1000-3000 j.m./dobę
- w niedoczynności przytarczyc i rzekomej niedoczynności przytarczyc 10 000-20 000 j.m./dobę w zależności od stężenia wapnia w surowicy
Stężenie wapnia we krwi należy kontrolować co 4-6 tygodni, następnie co 3-6 miesięcy.
Przypisy
edytuj- ↑ Ann R. Webb, Who, what, where and when-influences on cutaneous vitamin D synthesis, „Progress in Biophysics and Molecular Biology”, 92 (1), 2006, s. 17–25, DOI: 10.1016/j.pbiomolbio.2006.02.004, PMID: 16766240.
- ↑ David E. Prosser, Glenville Jones, Enzymes involved in the activation and inactivation of vitamin D, „Trends in Biochemical Sciences”, 29 (12), 2004, s. 664–673, DOI: 10.1016/j.tibs.2004.10.005, PMID: 15544953.
- ↑ a b Michael F. Holick, Vitamin D deficiency, „The New England Journal of Medicine”, 357 (3), 2007, s. 266–281, DOI: 10.1056/NEJMra070553, PMID: 17634462.
- ↑ F.M. Gloth i inni, Can vitamin D deficiency produce an unusual pain syndrome?, „Archives of Internal Medicine”, 151 (8), 1991, s. 1662–1664, PMID: 1872673.
- ↑ Gregory A. Plotnikoff, Joanna M. Quigley, Prevalence of severe hypovitaminosis D in patients with persistent, nonspecific musculoskeletal pain, „Mayo Clinic Proceedings”, 78 (12), 2003, s. 1463–1470, DOI: 10.4065/78.12.1463, PMID: 14661675.
- ↑ Nithya Anand, S.C. Chandrasekaran, Narpat Singh Rajput, Vitamin D and periodontal health: Current concepts, „Journal of Indian Society of Periodontology”, 17 (3), 2013, s. 302–308, DOI: 10.4103/0972-124X.115645, ISSN 0972-124X, PMID: 24049329, PMCID: PMC3768179 [dostęp 2018-06-18].
- ↑ Stein Sid, David Tipton, Vitamin D and its impact on oral health – an update, t. 91, 1 marca 2011 [dostęp 2018-06-18].
- ↑ Marta Michalska-Kasiczak i inni, Analysis of vitamin D levels in patients with and without statin-associated myalgia – a systematic review and meta-analysis of 7 studies with 2420 patients, „International Journal of Cardiology”, 178, 2015, s. 111–116, DOI: 10.1016/j.ijcard.2014.10.118, ISSN 1874-1754, PMID: 25464233 [dostęp 2018-06-17].
- ↑ David E. McCarty i inni, The link between vitamin D metabolism and sleep medicine, „Sleep Medicine Reviews”, 18 (4), 2014, s. 311–319, DOI: 10.1016/j.smrv.2013.07.001, PMID: 24075129.
- ↑ David E. McCarty i inni, Vitamin D, race, and excessive daytime sleepiness, „Journal of clinical sleep medicine: JCSM”, 8 (6), 2012, s. 693–697, DOI: 10.5664/jcsm.2266, PMID: 23243403, PMCID: PMC3501666.
- ↑ Wouter G Staal, Autism, Vitamin D and Early Brain Development, „Human Genetics & Embryology”, 6 (2), 2016, DOI: 10.4172/2161-0436.1000e114.
- ↑ Tian-Tian Wang i inni, Cutting edge: 1,25-dihydroxyvitamin D3 is a direct inducer of antimicrobial peptide gene expression, „Journal of Immunology (Baltimore, Md.: 1950)”, 173 (5), 2004, s. 2909–2912, DOI: 10.4049/jimmunol.173.5.2909, PMID: 15322146.
- ↑ Dima A Youssef i inni, Antimicrobial implications of vitamin D, „Dermato-endocrinology”, 3 (4), 2011, s. 220–229, DOI: 10.4161/derm.3.4.15027, ISSN 1938-1972, PMID: 22259647, PMCID: PMC3256336 [dostęp 2018-06-18].
- ↑ Center for Food Safety and Applied Nutrition, Constituent Updates – FDA Denies Qualified Health Claim Petition for Intake of Vitamin D to Reduce the Risk of Multiple Sclerosis in Healthy People [online], www.fda.gov [dostęp 2018-06-18] (ang.).
- ↑ Katharine Harding i inni, Seasonal variation in multiple sclerosis relapse, „Journal of Neurology”, 264 (6), 2017, s. 1059–1067, DOI: 10.1007/s00415-017-8485-0, ISSN 0340-5354, PMID: 28424900, PMCID: PMC5486559 [dostęp 2018-06-18].
- ↑ D. Michal Freedman i inni, Prospective study of serum vitamin D and cancer mortality in the United States, „Journal of the National Cancer Institute”, 99 (21), 2007, s. 1594–1602, DOI: 10.1093/jnci/djm204, PMID: 17971526.
- ↑ Philippe Autier, Sara Gandini, Vitamin D supplementation and total mortality: a meta-analysis of randomized controlled trials, „Archives of Internal Medicine”, 167 (16), 2007, s. 1730–1737, DOI: 10.1001/archinte.167.16.1730, PMID: 17846391.
- ↑ J.J. Cannell i inni, Epidemic influenza and vitamin D, „Epidemiology and Infection”, 134 (6), 2006, s. 1129–1140, DOI: 10.1017/S0950268806007175, PMID: 16959053, PMCID: PMC2870528.
- ↑ John J. Cannell i inni, On the epidemiology of influenza, „Virology Journal”, 5, 2008, s. 29, DOI: 10.1186/1743-422X-5-29, PMID: 18298852, PMCID: PMC2279112.
- ↑ Varshil Mehta, Shivika Agarwal, Does Vitamin D Deficiency Lead to Hypertension?, „Cureus”, 9 (2), DOI: 10.7759/cureus.1038, ISSN 2168-8184, PMID: 28357170, PMCID: PMC5356990 [dostęp 2018-06-17].
- ↑ Dan Qi i inni, Vitamin D and hypertension: Prospective study and meta-analysis, „PLoS ONE”, 12 (3), 2017, DOI: 10.1371/journal.pone.0174298, ISSN 1932-6203, PMID: 28358827, PMCID: PMC5373576 [dostęp 2018-06-17].
- ↑ Stefanie S Schleithoff i inni, Vitamin D supplementation improves cytokine profiles in patients with congestive heart failure: a double-blind, randomized, placebo-controlled trial, „The American Journal of Clinical Nutrition”, 83 (4), 2006, s. 754–759, DOI: 10.1093/ajcn/83.4.754, ISSN 0002-9165 [dostęp 2018-06-17] (ang.).
- ↑ Kunachowicz H., Nadolna I., Przygoda B. i wsp.: Tabele składu i wartości odżywczej żywności. Wydawnictwo Lekarskie PZWL. Warszawa, 2005.
- ↑ Normy żywienia opublikowane przez Instytut Żywności i Żywienia. izz.waw.pl. [zarchiwizowane z tego adresu (2008-06-14)]. (dostęp 2008-02-10).
- ↑ Vitamins: what they do and where to find them (EUFIC). [w:] European Food Information Council [on-line]. 2010-12-10. [dostęp 2010-12-11]. [zarchiwizowane z tego adresu (2011-10-02)]. Cytat: Vitamin D
- ↑ 14. Appendix F: Calculate the Percent Daily Value for the Appropriate Nutrients. Food and Drug Administration, 2011 (data ostatniej aktualizacji). [dostęp 2011-11-13]. (ang.).
- ↑ Institute of Medicine, Food and Nutrition Board. Dietary Reference Intakes: Calcium, Phosphorus, Magnesium, Vitamin D and Fluoride. National Academy Press, Washington, DC, 1999.
- ↑ B. Dawson-Hughes i inni, IOF position statement: vitamin D recommendations for older adults, „Osteoporosis international”, 21 (7), 2010, s. 1151–1154, DOI: 10.1007/s00198-010-1285-3, PMID: 20422154.
- ↑ Vitamin D: Vitamin Deficiency, Dependency, and Toxicity: Merck Manual Professional.
- ↑ Dietary Supplement Fact Sheet: Vitamin D. Office of Dietary Supplements, National Institutes of Health, 2009-11-13. [dostęp 2010-11-04].
- ↑ Dietary Reference Intakes for Calcium and Vitamin D. iom.edu. [zarchiwizowane z tego adresu (2015-06-20)]. Institute of Medicine.
- ↑ Nutrition advice: The vitamin D-lemma Nature News & Comment.
- ↑ Interna Szczeklika 2016, red. Piotr Gajewski, wersja elektroniczna, dostęp 2016-10-07.
- ↑ a b Marian L. Evatt i inni, Prevalence of vitamin d insufficiency in patients with Parkinson disease and Alzheimer disease, „Archives of Neurology”, 65 (10), 2008, s. 1348–1352, DOI: 10.1001/archneur.65.10.1348, PMID: 18852350, PMCID: PMC2746037.
- ↑ Mikołaj Kamiński i inni, Insulin Resistance in Adults with Type 1 Diabetes is Associated with Lower Vitamin D Serum Concentration, „Experimental and Clinical Endocrinology & Diabetes”, 2019, Epub ahead of print, DOI: 10.1055/a-0895-5166, PMID: 31049899 (ang.).
- ↑ Dietary Supplement Fact Sheet: Vitamin D.
- ↑ a b Agnieszka Rusińska i inni, Zasady suplementacji leczenia witaminą D - Nowelizacja 2018, „Postępy Neonatologii”, 24(1), 2018, s. 1-24 [dostęp 2021-08-26] (pol.).
- ↑ Scientific Opinion on the Tolerable Upper Intake Level of vitamin D, „European Food Safety Authority” [dostęp 2018-06-18] (ang.).
- ↑ „Świat Nauki”. Styczeń 2008 (197), 2008. Warszawa: Prószyński Media Sp. z o.o.. ISSN 08676380.
- ↑ Jerzy Wicha, Droga pod słońce. Wczesna historia witaminy D. Wiadomości Chemiczne, 2012, 66 (7-8), 671-696.
- ↑ E.V. McCollum i inni, The effect of additions of fluorine to the diet of the rat on the quality of the teeth. 1925. Studies on experimental rickets. XXI. An experimental demonstration of the existence of a vitamin which promotes calcium deposition. 1922. The effect of additions of fluorine to the diet of the rat on the quality of the teeth. 1925, „Journal of Biological Chemistry”, 277 (19), 2002, E8, PMID: 11991957.
- ↑ J.W. Blunt, H.F. DeLuca, H.K. Schnoes, 25-hydroxycholecalciferol. A biologically active metabolite of vitamin D3, „Biochemistry”, 7 (10), 1968, s. 3317–3322, DOI: 10.1021/bi00850a001, PMID: 4300699.
- ↑ a b Ewa Marcinowska-Suchowierska, Paweł Płudowski, Niedobory witaminy D u osób dorosłych [online], Medycyna po Dyplomie, 2018 [dostęp 2021-01-19].
Bibliografia
edytuj- Hanna Myśliwiec, Michał Myśliwiec. Rola witaminy D w ustroju. „Medycyna po Dyplomie”. Wrzesień 2007. 16/9, s. 130–135, 2007.
- Luz Tavera-Mendoza, John White. Słoneczna tarcza. „Świat Nauki”. Styczeń 2008. 1 (197). s. 34–41.
- Dobrzańska A. i Zespół Ekspertów Polskie zalecenia dotyczące profilaktyki niedoborów witaminy D – 2009
- Zdzisław Sikorski, Chemia żywności, Wydawnictwa Naukowo-Techniczne. Warszawa 2000. ISBN 83-204-2448-8.
- Justyna Kosińska, Katarzyna Billing-Marczak, Marcin Krotkiewski. Nowe nieznane funkcje witaminy D. „Medycyna Rodzinna”, s. 34–47, 2008.