Wirus zapalenia wątroby typu C
Wirus zapalenia wątroby typu C (WZW C, ang. hepatitis C virus, HCV) – otoczkowy wirus ssRNA z rodziny Flaviviridae, rodzaju Hepacivirus. Jego średnica wynosi około 60–70 nanometrów.
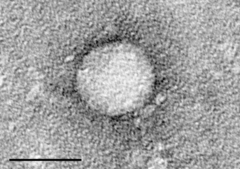 Wirus zapalenia wątroby typu C widoczny w mikroskopie elektronowym | |
| Systematyka | |
| Grupa |
Grupa IV ((+)ssRNA) |
|---|---|
| Rodzina |
Flaviviridae |
| Rodzaj |
Hepacivirus |
| Nazwa systematyczna | |
| Hepatitis C Virus | |
| Cechy wiralne | |
| Skrót |
HCV |
| Kwas nukleinowy |
RNA |
| Liczba nici |
jedna |
| Polaryzacja kwasu nukleinowego |
dodatnia |
| Osłonka |
obecna |
| Nagi kwas nukleinowy |
zakaźny |
| Rezerwuar |
człowiek |
| Wywoływane choroby | |
HCV wywołuje wirusowe zapalenie wątroby typu C, którego konsekwencją jest pozapalna marskość wątroby i rak wątrobowokomórkowy (pierwotny rak wątroby). HCV jest zdolny do wywołania nosicielstwa. Wykazuje dużą wrażliwość na środki i metody dezynfekcyjne, większą niż HBV, mniejszą niż HIV.
Historia
edytujWirus HCV został zidentyfikowany dopiero w 1989 roku, choć wcześniej wiedziano, że musi istnieć czynnik wywołujący zapalenia wątroby określanej jako nie-A-nie-B (NANB hepatitis). W późniejszym okresie wykryto także kolejne wirusy zapalenia wątroby nazwane HGV, GB-C i TTV. Badania nad ich wpływem na wątrobę trwają.
Odkrycia wirusa HCV dokonały zespoły kierowane przez Harveya Altera, Michaela Houghtona oraz Charles'a Rice'a – za co w 2020 roku, zostali uhonorowani Nagrodą Nobla.
Epidemiologia
edytujWedług danych Państwowego Zakładu Higieny i Instytutu Hematologii i Transfuzjologii, uznawanych przez WHO, szacuje się, że w Polsce zakażone jest około 1,4% populacji; wśród dawców krwi przeciwciała anty-HCV wykrywa się u 0,5% osób. W akcjach Stowarzyszenie „Prometeusze”, bezpłatnych badaniach przesiewowych, organizowanych od 2005 roku, wykryto w sumie około 1,75% zakażeń wśród populacji polskiej (dodatnie wyniki przeciwciał anty-HCV). Wśród kobiet ciężarnych w 2007 roku wykryto odsetek mniejszy od 0,5% (8 wyników dodatnich na 1585 badań).
Szacuje się, że w Polsce HCV zakażonych jest około 200 tys.[1] osób dorosłych, a na świecie około 170 mln[2]. Genotypem dominującym w Polsce jest 1B (ok. 80% przypadków zakażeń), przy którym skuteczność leczenia wynosi 56-57%. HCV to bardzo poważny problem medyczny i społeczny. Wykryto dotychczas zaledwie pomiędzy 20 a 50 tys. zakażonych (dane Polskiej Grupy Ekspertów HCV – 20 tys. versus dane Stowarzyszenia "Prometeusze" – 50 tys.), co stanowi bardzo niewielki odsetek wykrywalności. Przyczyna leży po stronie bezoobjawowości zakażenia, które nawet do 20–30 lat może się nie ujawniać. Nieleczone przewlekłe zakażenie HCV prowadzić może do marskości i raka pierwotnego tego narządu. Wiedza społeczeństwa o HCV jest bardzo niska – w badaniu opinii publicznej (TNS OBOP wrzesień 2007 rok) ok. 93% społeczeństwa nie wiedziało co to jest HCV. W obliczu braku szczepionki przeciw HCV leczenie jest jedyną formą przeciwdziałania szerzeniu się epidemii – zmniejszenie rezerwuaru HCV w populacji. Leczenie jest refundowane w ramach tak zwanych programów lekowych. Aby wykryć zakażenie HCV, należy zacząć od prostego testu serologicznego.
Leczenie
edytujLeczenie HCV w Polsce odbywa się w ramach programu lekowego[3] Ministerstwa Zdrowia i jest w pełni refundowane. Przed rozpoczęciem leczenia każdy pacjent ma rozszerzoną diagnostykę laboratoryjną w której bada się m.in.
- genotyp wirusa
- obecność autoprzeciwciał: ANA, AMA, ASMA, LKM
- choroby współistniejące, szczególnie choroby przewlekłe takie jak nawracające depresje, padaczka, choroby autoimmunologiczne
- czynność tarczycy (TSH, T4, T3)
- rozszerzoną morfologię
- badanie biochemiczne krwi
- biopsję wątroby celem określenia stopnia aktywności zapalnej choroby (grading) i zmian trwałych w wątrobie - zasięgu włóknienia (staging) lub fibroscan.
- wielkość wiremii wyjściowej - metodą PCR.
Po ustaleniu wskazań pacjent kierowany jest do leczenia - zwykle w ramach oddziału dziennego. Na chwilę obecną (rok 2015) leczenie polega na stosowaniu:
- interferonu pegylowanego alfa-2 (Pegasys Peginterferon alfa-2a, Pegintron Peginterferon alfa-2b) podawanego podskórnie raz na tydzień, zwykle w dawce 180 μg
- rybawiryny podawanej doustnie w dawkach zwykle od 800 do 1200 mg na dobę
Ponadto u pacjentów spełniających określone kryteria stosuje się:
- boceprewir, telaprewir lub symeprewir, będące inhibitorami proteaz (dopuszczone do leczenia WZW C przez amerykańską Agencję Żywności i Leków[4])
- sofosbuwir
Od 1 listopada 2015 roku refundowane są również terapie bezinterferonowe, charakteryzujące się wysokim współczynnikiem (ponad 90%) wyleczeń oraz małą możliwością wystąpienia skutków ubocznych. Obecnie (2015) w refundacji są:
- daklataswir
- Viekirax (parytaprewir, rytonawir, ombitaswir), Exviera (dazabuwir)
- Harvoni (sofosbuwir, ledipaswir)
Leczenie interferonowe jest obarczone ryzykiem wielu skutków ubocznych, z których najczęstsze to:
- chroniczne zmęczenie, bóle mięśni, stawów, gorączka, bóle głowy
- zmiany w morfologii krwi (anemia, neutropenia, trombocytopenia, hyperurykemia)
- zmianami psychicznymi (dysforia, bezsenność, depresja)
- uczulenia, wysychanie śluzówek, kaszel, suchość skóry.
Intensywność odczuwania objawów ubocznych jest uzależniona od osobniczej wrażliwości organizmu na zastosowane leczenie. Stosuje się leki korygujące objawy uboczne, na przykład paracetamol, NLPZ, środki kosmetyczne nawilżające i natłuszczające. Groźne skutki uboczne (silna anemia, silna neutropenia) wymagają czasem redukcji dawek leków.
Proliferację wirusa hamuje enzym - palmitylotransferaza seryny (SPT), poprzez wzmożoną produkcję sfingolipidów, wiążących się z kompleksami białkowymi wirusa. Badania z 2013 roku, przeprowadzone na mysich chimerach z ludzkimi wątrobami, sugerują potencjalne zastosowanie SPT jako nowej metody leczenia[5].
Choroba
edytujWiększość (96%) zakażonych nie jest świadoma swojego stanu, ponieważ zazwyczaj przewlekła infekcja jest skąpoobjawowa i trwa latami. Średni czas trwania zakażenia HCV, od momentu wniknięcia wirusa do ustroju do poważnych problemów zdrowotnych, jest zazwyczaj dłuższy niż w przypadku HIV i trwa 5 do 35 lat. Choroba często kończy się marskością i rakiem wątroby, poprzedzonymi poważnymi komplikacjami, uniemożliwiającymi normalne funkcjonowanie (wodobrzusze, żylaki i krwawienia przełyku, żółtaczka, problemy z krzepliwością krwi, zaburzenia psychiczne, do śpiączki wątrobowej włącznie). Zapaleniu wątroby, wywołanemu przez HCV, często towarzyszą choroby autoimmunologiczne, w tym autoimmunologiczne zapalenie wątroby (AIH), które znacznie pogarszają rokowanie i czas przeżycia.
Drogi i mechanizm zakażenia
edytujŹródło zakażenia stanowią ludzie chorzy na WZW i nosiciele. HCV przenosi się podczas kontaktu krwi własnej z krwią nosiciela. Potencjalnie zakaźny jest każdy materiał zawierający krew. Wirus przenosi się w czasie zabiegów medycznych: pobierania i transfuzji krwi, zabiegów operacyjnych i innych, a także przez zabiegi niemedyczne, takie jak wykonywanie tatuażu, wstrzykiwanie narkotyku niesterylną igłą lub strzykawką itd. Prawdopodobieństwo zakażenia przez produkty krwiopochodne wynosi 3,3%. Możliwość okołoporodowej transmisji wirusa z matki na noworodka wynosi około 5-6%. Jak dotąd nie znaleziono skutecznej szczepionki przeciw HCV. W wielu przypadkach możliwe jest zahamowanie działalności wirusa w organizmie, a nawet zahamowanie procesu jego namnażania, dzięki takim środkom jak interferon i rybawiryna. W trakcie badań jest szereg nowych leków, takich jak wiramidyna czy kwas lukrecjowy.
Do zakażenia HCV najczęściej dochodzi podczas zabiegów medycznych:
- operacji, zabiegów chirurgicznych, badań (np. bronchoskopia)
- zabiegów stomatologicznych
- zastrzyków
- pobierania krwi bez zmiany rękawiczek przez pielęgniarkę
- dializ[6]
- przyjmowania produktów krwiopochodnych i przeszczepiania narządów (zwłaszcza przed 1992)
- usuwania znamion.
Można się też zakazić podczas:
- manikiuru, pedikiuru
- wizyty u fryzjera (zranienie brzytwą, żyletką, nożyczkami)
- akupunktury
- używania tych samych przyborów kosmetycznych przez członków rodziny
- robienia tatuaży[6]
- przekłuwania uszu lub kolczykowania ciała[6]
- bójki (jeśli doszło do kontaktu z krwią)
- uprawiania sportów kontaktowych (boks, piłka nożna, koszykówka), jeśli doszło do uszkodzenia ciała
- stosunku seksualnego (prawdopodobieństwo zarażenia się HCV od monogamicznego partnera heteroseksualnego wynosi maksymalnie 0,07% rocznie – jedno zakażenie następuje na 190 000 stosunków[7]), ryzyko rośnie w przypadku kontaktów z przypadkowymi partnerami[8] oraz w przypadku MSM[9]
- praktyk sado-maso
- skaleczeń, ran, zadrapań podczas naprawiania sprzętu (zwłaszcza medycznego)
- używania dożylnie narkotyków[6]
- używania iniekcyjnych środków dopingujących
- ciąży i porodu
- udzielania pierwszej pomocy ofiarom wypadków bez zachowania należytego zabezpieczenia
- pracy z chorymi na HCV, bez zachowania należytego bezpieczeństwa przy kontakcie z krwią
- pracy z materiałem zakaźnym (np. w laboratorium) bez zachowania zasad bezpieczeństwa.
W przypadku każdego kontaktu z krwią osoby zakażonej może dojść do infekcji.
Zaliczanie zakażenia HCV do chorób przenoszonych drogą płciową jest kontrowersyjne[10]. Ryzyko zakażenia przez kontakty seksualne istnieje, chociaż jest niskie[11], ze względu na możliwość uszkodzenia naskórka i/lub błony śluzowej narządów rodnych np. w czasie stosunków analnych. Wśród stałych partnerów HCV częstość występowania HCV wynosi 2-4%[7][12][13]. Ryzyko rośnie wraz z ilością partnerów seksualnych[8]. Ryzyko zakażenia u homoseksualnych mężczyzn jest większe, jeżeli występuje koinfekcja HIV. Jakkolwiek materiał genetyczny wirusa można wykryć w nasieniu, sperma osób zakażonych nie transmituje wirusa[14].
Wirus HCV nie przenosi się przez:
- kichanie i kaszel
- trzymanie za ręce
- całowanie się
- używanie tej samej toalety, wanny, prysznica
- spożywanie żywności przygotowywanej przez osobę zakażona HCV (jeżeli żywność nie miała kontaktu z krwią tej osoby)
- trzymanie kogoś w objęciach, przytulanie
- pływanie w tym samym zbiorniku wodnym
- zabawę z dziećmi, sport (jeśli nie dochodzi do uszkodzeń ciała).
W USA około 30% osób zakażonych HIV jest także zakażonych HCV ze względu na podobne drogi przenoszenia się wirusów[15].
Diagnostyka pacjentów zakażonych HCV jest refundowana przez Narodowy Fundusz Zdrowia. Aby wykonać bezpłatnie podstawowy test serologiczny w kierunku obecności wirusa HCV wymagane jest skierowanie od lekarza chorób zakaźnych (w przypadku kobiet w ciąży skierowanie może wystawić lekarz ginekolog).
Prywatnie test oznaczenia przeciwciał anty-HCV oferowany jest w większości laboratoriów w Polsce w cenie ok. 30–40 zł.
Światowy Dzień Wirusowego Zapalenia Wątroby
edytujŚwiatowy Dzień Wirusowego Zapalenia Wątroby (WHD, z ang. World Hepatitis Day) jest obchodzony 28 lipca, w dzień urodzin Barucha Samuela Blumberga, który zidentyfikował wirusa zapalenia wątroby typu B.
Zobacz też
edytujPrzypisy
edytuj- ↑ HCV jestem świadom [online], www.hcv.pzh.gov.pl [dostęp 2017-11-27].
- ↑ Andrzej Szczeklik: Choroby wewnętrzne [Dokument elektroniczny] : podręcznik multimedialny oparty na zasadach EBM. Kraków: Medycyna Praktyczna, 2006. ISBN 83-7430-072-8.
- ↑ Programy lekowe | Ministerstwo Zdrowia [online], www.mz.gov.pl [dostęp 2017-11-27] (pol.).
- ↑ Jessica Wapner. Cel - proteaza. „Świat Nauki”. nr. 9 (241), s. 11, wrzesień 2011. Prószyński Media. ISSN 0867-6380.
- ↑ Asao Katsume i inni, A serine palmitoyltransferase inhibitor blocks hepatitis C virus replication in human hepatocytes, „Gastroenterology”, 145 (4), 2013, s. 865–873, DOI: 10.1053/j.gastro.2013.06.012, ISSN 1528-0012, PMID: 23791700 [dostęp 2017-02-08].
- ↑ a b c d prof. dr hab. n. med. Anna Boroń–Kaczmarska: Drogi zakażenia HCV. [dostęp 2009-03-21]. (pol.).
- ↑ a b NA. Terrault, JL. Dodge, EL. Murphy, JE. Tavis i inni. Sexual transmission of hepatitis C virus among monogamous heterosexual couples: the HCV partners study.. „Hepatology”. 57 (3), s. 881-9, Mar 2013. DOI: 10.1002/hep.26164. PMID: 23175457.
- ↑ a b A. Mele, T. Stroffolini, ME. Tosti, R. Corona i inni. Heterosexual transmission of hepatitis C in Italy.. „J Med Virol”. 57 (2), s. 111-3, Feb 1999. PMID: 9892393.
- ↑ CDC: Hepatitis C. [dostęp 2014-07-14]. (ang.).
- ↑ Norah A. Terrault i inni, Sexual transmission of hepatitis C virus among monogamous heterosexual couples: the HCV partners study, „Hepatology (Baltimore, Md.)”, 57 (3), 2013, s. 881–889, DOI: 10.1002/hep.26164, ISSN 1527-3350, PMID: 23175457, PMCID: PMC4384338 [dostęp 2017-04-13].
- ↑ GP. Hammer, TA. Kellogg, WC. McFarland, E. Wong i inni. Low incidence and prevalence of hepatitis C virus infection among sexually active non-intravenous drug-using adults, San Francisco, 1997-2000.. „Sex Transm Dis”. 30 (12), s. 919-24, Dec 2003. DOI: 10.1097/01.OLQ.0000091152.31366.E6. PMID: 14646642.
- ↑ V. Tahan, C. Karaca, B. Yildirim, A. Bozbas i inni. Sexual transmission of HCV between spouses.. „Am J Gastroenterol”. 100 (4), s. 821-4, Apr 2005. DOI: 10.1111/j.1572-0241.2005.40879.x. PMID: 15784025.
- ↑ KM. Roy, DJ. Goldberg, S. Hutchinson, SO. Cameron i inni. Hepatitis C virus among self declared non-injecting sexual partners of injecting drug users.. „J Med Virol”. 74 (1), s. 62-6, Sep 2004. DOI: 10.1002/jmv.20146. PMID: 15258969.
- ↑ HCV in Semen [online], www.natap.org [dostęp 2017-04-13].
- ↑ HOME | www.hivandhepatitis.com [online], www.hivandhepatitis.com [dostęp 2017-11-27] (ang.).
Bibliografia
edytujLinki zewnętrzne
edytuj
|